Acidul sulfuric (H2SO4) este unul dintre cei mai corozivi acizi și reactivi periculoși cunoscuți de om, în special sub formă concentrată. Acidul sulfuric chimic pur este un lichid toxic greu, cu consistență uleioasă, inodor și incolor. Se obține prin metoda de oxidare a dioxidului de sulf (SO2) prin metoda de contact.
La o temperatură de + 10,5 ° C, acidul sulfuric se transformă într-o masă cristalină sticloasă solidificată, cu lăcomie, ca un burete, absorbind umezeala din mediu. În industrie și chimie, acidul sulfuric este unul dintre principalii compuși chimici și ocupă o poziție de lider în ceea ce privește producția în tone. De aceea acidul sulfuric este numit „sângele chimiei”. Cu ajutorul acidului sulfuric, îngrășăminte, medicamente, alți acizi, se obține o gamă largă de substanțe chimice, îngrășăminte și multe altele.

Proprietățile fizice și chimice de bază ale acidului sulfuric
- Acidul sulfuric pur (formula H2SO4), la o concentrație de 100%, este un lichid gros și incolor. Cea mai importantă proprietate a H2SO4 este higroscopicitatea ridicată - este capacitatea de a elimina apa din aer. Acest proces este însoțit de o degajare de căldură pe scară largă.
- H2SO4 este un acid puternic.
- Acidul sulfuric se numește monohidrat - există 1 mol de H2O (apă) la 1 mol de SO3. Datorită proprietăților sale higroscopice impresionante, este folosit pentru a extrage umezeala din gaze.
- Punctul de fierbere este de 330 ° C. În acest caz, acidul se descompune în SO3 și apă. Densitate - 1,84. Punct de topire - 10,3 ° C /.
- Acidul sulfuric concentrat este un agent oxidant puternic. Acidul trebuie încălzit pentru a începe reacția redox. Rezultatul reacției este SO2. S + 2H2SO4 = 3SO2 + 2H2O
- În funcție de concentrație, acidul sulfuric reacționează diferit cu metalele. Într-o stare diluată, acidul sulfuric este capabil să oxideze toate metalele care se află în intervalul de tensiuni la hidrogen. Excepția este platina și aurul ca fiind cele mai rezistente la oxidare. Acidul sulfuric diluat reacționează cu sărurile, bazele, oxizii amfoteri și bazici. Acidul sulfuric concentrat este capabil să oxideze toate metalele într-o serie de tensiuni, iar argintul este, de asemenea.
- Acidul sulfuric formează două tipuri de săruri: acidă (acestea sunt hidrosulfați) și medie (sulfați)
- H2SO4 reacționează activ cu substanțele organice și nemetalele, iar unele dintre ele se pot transforma în cărbune.
- Anhidritul sulfuric se dizolvă perfect în H2SO4 și se formează oleum - o soluție de SO3 în acid sulfuric. În exterior, arată astfel: fumurarea acidului sulfuric, care eliberează anhidrit sulfuric.
- Acidul sulfuric din soluțiile apoase este un dibazic puternic și, atunci când este adăugat în apă, se eliberează o cantitate imensă de căldură. Când soluțiile diluate de H2SO4 sunt preparate din soluții concentrate, este necesar să adăugați un acid mai greu în apă într-un curent mic și nu invers. Acest lucru se face pentru a evita fierberea apei și stropirea acidă.
Acizi sulfurici concentrati si diluati
Soluțiile concentrate de acid sulfuric includ soluții de la 40%, capabile să dizolve argint sau paladiu.
Acidul sulfuric diluat include soluții a căror concentrație este mai mică de 40%. Acestea nu sunt astfel de soluții active, dar sunt capabile să reacționeze cu alamă și cupru.
Producerea acidului sulfuric
Producția de acid sulfuric la scară industrială a fost lansată în secolul al XV-lea, dar în acel moment se numea „ulei vitriol”. Dacă omenirea mai devreme consuma doar câteva zeci de litri de acid sulfuric, atunci în lumea modernă calculul ajunge la milioane de tone pe an.
Acidul sulfuric este produs industrial și există trei dintre ele:
- Metoda de contact.
- Mod azotat
- Alte metode
Să vorbim în detaliu despre fiecare dintre ele.
Contactați metoda de producție
Metoda de contact de producție este cea mai comună și îndeplinește următoarele sarcini:
- Rezultă un produs care satisface nevoile numărului maxim de consumatori.
- Reducerea daunelor asupra mediului în timpul producției.
În metoda de contact, următoarele substanțe sunt utilizate ca materii prime:
- pirita (pirita de sulf);
- sulf;
- oxid de vanadiu (această substanță acționează ca un catalizator);
- sulfat de hidrogen;
- sulfuri de diferite metale.
Înainte de a începe procesul de producție, materiile prime sunt pregătite în prealabil. Pentru început, pirita este zdrobită în instalații speciale de zdrobire, ceea ce permite, datorită creșterii zonei de contact a substanțelor active, să accelereze reacția. Pirita este purificată: este scufundată în recipiente mari de apă, timp în care plutesc la suprafață rocile reziduale și tot felul de impurități. Acestea sunt eliminate la sfârșitul procesului.
Partea de producție este împărțită în mai multe etape:
- După zdrobire, pirita este purificată și trimisă în cuptor, unde este arsă la temperaturi de până la 800 ° C. Conform principiului contracurentului, aerul este introdus în cameră de jos și acest lucru asigură pirita în stare suspendată. Astăzi, acest proces durează câteva secunde, dar mai devreme a durat câteva ore pentru a arde. În timpul procesului de prăjire, deșeurile apar sub formă de oxid de fier, care sunt îndepărtate și apoi transferate în industria metalurgică. Arderea produce vapori de apă, gaze O2 și SO2. Când purificarea de vapori de apă și cele mai mici impurități este finalizată, se obține oxid de sulf pur și oxigen.
- În a doua etapă, are loc o reacție exotermă sub presiune folosind un catalizator de vanadiu. Reacția începe atunci când temperatura atinge 420 ° C, dar poate fi crescută la 550 ° C pentru a crește eficiența. În timpul reacției are loc oxidarea catalitică și SO2 devine SO3.
- Esența celei de-a treia etape de producție este următoarea: absorbția SO3 în turnul de absorbție, în timpul căruia se formează oleum H2SO4. În această formă, H2SO4 este turnat în recipiente speciale (nu reacționează cu oțelul) și este gata să se întâlnească cu utilizatorul final.
În timpul producției, așa cum am spus mai sus, se generează multă energie termică, care este utilizată pentru încălzire. Multe instalații cu acid sulfuric instalează turbine cu abur care utilizează aburul emis pentru a genera electricitate suplimentară.
Metoda azotată pentru producerea acidului sulfuric
În ciuda avantajelor metodei de producție de contact, în care se obțin acid sulfuric și oleum mai concentrat și pur, se obține o mulțime de H2SO4 prin metoda azotată. În special, la plantele cu superfosfat.
Pentru producerea de H2SO4, dioxidul de sulf acționează ca materie primă atât în metoda de contact, cât și în cea azotată. Se obține special în aceste scopuri prin arderea sulfului sau arderea metalelor sulfuroase.
Prelucrarea dioxidului de sulf în acid sulfuric constă în oxidarea dioxidului de sulf și adăugarea de apă. Formula arată astfel:
SO2 + 1 | 2 O2 + H2O = H2SO4
Dar dioxidul de sulf nu reacționează direct cu oxigenul, prin urmare, cu metoda azotată, dioxidul de sulf este oxidat folosind oxizi de azot. Oxizi de azot mai mari (vorbim despre dioxid de azot NO2, trioxid de azot NO3) în timpul acestui proces sunt reduși la oxid de azot NO, care este apoi oxidat din nou de oxigen la oxizi mai mari.
Producția de acid sulfuric prin metoda azotată este formalizată tehnic în două moduri:
- Cameră.
- Turn.
Metoda azotată are o serie de avantaje și dezavantaje.
Dezavantaje ale metodei azotate:
- Se dovedește 75% acid sulfuric.
- Calitatea produsului este scăzută.
- Revenirea incompletă a oxizilor de azot (adăugarea de HNO3). Emisiile lor sunt dăunătoare.
- Acidul conține fier, oxizi de azot și alte impurități.
Avantajele metodei azotate:
- Cost de proces mai mic.
- 100% reciclare SO2.
- Simplitatea designului hardware.
Principalele plante rusești pentru producerea de acid sulfuric
Producția anuală de H2SO4 în țara noastră este calculată în șase cifre - este de aproximativ 10 milioane de tone. Principalii producători de acid sulfuric din Rusia sunt companiile, care, în plus, sunt principalii săi consumatori. Vorbim despre companii al căror domeniu de activitate este producția de îngrășăminte minerale. De exemplu, „Îngrășăminte minerale Balakovo”, „Ammophos”.

Cel mai mare producător de dioxid de titan din Europa de Est, Crimeea Titan, operează în Armyansk în Crimeea. În plus, planta se ocupă cu producerea de acid sulfuric, îngrășăminte minerale, sulfat feros etc.
Acidul sulfuric de diferite tipuri este produs de multe fabrici. De exemplu, acidul sulfuric pe baterie este produs de: Karabashmed, FKP Biysk Oleum Plant, Svyatogor, Slavia, Severkhimprom etc.
Oleum este produs de UCC Shchekinoazot, FKP Biysk Oleum Plant, Ural Mining and Metalurgical Company, PO Kirishinefteorgsintez etc.
Acidul sulfuric de înaltă puritate este produs de OHK Shchekinoazot, component-reactiv.
Acidul sulfuric uzat poate fi cumpărat la fabricile ZSS, HaloPolymer Kirovo-Chepetsk.
Producătorii de acid sulfuric tehnic sunt Promsintez, Khiprom, Svyatogor, Apatit, Karabashmed, Slavia, Lukoil-Permnefteorgsintez, Chelyabinsk Zinc Plant, Electrozinc etc.
Datorită faptului că pirita este principala materie primă în producția de H2SO4, iar aceasta este o risipă a întreprinderilor de îmbogățire, furnizorii săi sunt fabricile de îmbogățire Norilsk și Talnakh.
Liderii mondiali în producția de H2SO4 sunt ocupați de SUA și China, care reprezintă 30 de milioane de tone și respectiv 60 de milioane de tone.
Domeniul de aplicare a acidului sulfuric
Lumea consumă anual aproximativ 200 de milioane de tone de H2SO4, din care se produce o gamă largă de produse. Acidul sulfuric deține pe bună dreptate palma printre alți acizi în ceea ce privește utilizarea industrială.
După cum știți deja, acidul sulfuric este unul dintre cele mai importante produse ale industriei chimice, astfel încât domeniul de aplicare al acidului sulfuric este destul de larg. Principalele direcții de utilizare a H2SO4 sunt următoarele:
- Acidul sulfuric este utilizat în volume colosale pentru producerea de îngrășăminte minerale, iar acest lucru necesită aproximativ 40% din tonajul total. Din acest motiv, plantele H2SO4 sunt construite lângă plantele de îngrășăminte. Acestea sunt sulfat de amoniu, superfosfat etc. În producția lor, acidul sulfuric este luat în formă pură (concentrație 100%). Pentru a produce o tonă de amofos sau superfosfat, sunt necesari 600 de litri de H2SO4. Acești îngrășăminte sunt utilizate în majoritatea cazurilor în agricultură.
- H2SO4 este utilizat pentru producerea de explozivi.
- Rafinarea produselor petroliere. Pentru a obține kerosen, benzină, uleiuri minerale, este necesară purificarea hidrocarburilor, care are loc odată cu utilizarea acidului sulfuric. În procesul de rafinare a petrolului pentru purificarea hidrocarburilor, această industrie „ia” până la 30% din tonajul mondial de H2SO4. În plus, numărul octanic al combustibilului este crescut cu acid sulfuric, iar godeurile sunt tratate în timpul producției de petrol.
- În industria metalurgică. Acidul sulfuric în metalurgie este utilizat pentru a îndepărta solziul și rugina de pe sârmă, tablă, precum și pentru a restabili aluminiul în producția de metale neferoase. Înainte de a acoperi suprafețele metalice cu cupru, crom sau nichel, suprafața este gravată cu acid sulfuric.
- În producția de produse farmaceutice.
- În producția de vopsele.
- În industria chimică. H2SO4 este utilizat în producția de detergenți, alcool etilic, insecticide etc. și, fără acesta, aceste procese sunt imposibile.
- Pentru prepararea altor acizi, compuși organici și anorganici cunoscuți folosiți în scopuri industriale.
Sărurile acidului sulfuric și utilizarea lor
Cele mai importante săruri ale acidului sulfuric:
- Sarea Glauber Na2SO4 · 10H2O (sulfat de sodiu cristalin). Domeniul de aplicare al acesteia este destul de încăpător: producția de sticlă, sodă, în medicina veterinară și în medicină.
- Sulfatul de bariu BaSO4 este utilizat în producția de cauciuc, hârtie, vopsea minerală albă. În plus, este indispensabil în medicină pentru fluoroscopie gastrică. Se folosește pentru a face „terci de bariu” pentru această procedură.
- Sulfatul de calciu CaSO4. În natură, poate fi găsit sub formă de gips CaSO4 2H2O și anhidrit CaSO4. Gipsul CaSO4 · 2H2O și sulfatul de calciu sunt utilizate în medicină și construcții. Cu gips, atunci când este încălzit la o temperatură de 150 - 170 ° C, apare o deshidratare parțială, în urma căreia se obține gips ars, cunoscut de noi ca alabastru. Frământând alabastru cu apă până la consistența unui aluat, masa se întărește rapid și se transformă într-un fel de piatră. Această proprietate a alabastrului este utilizată în mod activ în lucrările de construcție: din aceasta se fac piese și matrițe. În lucrările de tencuială, alabastrul este de neînlocuit ca material de legare. Pacienților din departamentele de traumatisme li se administrează bandaje solide speciale de fixare - se fac pe bază de alabastru.
- Sulfatul de fier FeSO4 7H2O este utilizat pentru prepararea cernelii, impregnarea lemnului, precum și în activitățile agricole pentru distrugerea dăunătorilor.
- Alum KCr (SO4) 2 12H2O, KAl (SO4) 2 12H2O etc. sunt utilizate în producția de vopsele și în industria pielăriei (tăbăcirea pielii).
- Sulfat de cupru CuSO4 · 5H2O mulți dintre voi îl cunoașteți direct. Este un asistent activ în agricultură în lupta împotriva bolilor și dăunătorilor plantelor - o soluție apoasă de CuSO4 · 5H2O este utilizată pentru murarea cerealelor și pulverizarea plantelor. Se mai folosește și pentru prepararea unor vopsele minerale. Și în viața de zi cu zi este folosit pentru a îndepărta mucegaiul de pe pereți.
- Sulfatul de aluminiu - utilizat în industria celulozei și hârtiei.
Acidul sulfuric diluat este utilizat ca electrolit în bateriile cu plumb-acid. În plus, este folosit pentru a produce detergenți și îngrășăminte. Dar, în majoritatea cazurilor, vine sub formă de oleum - este o soluție de SO3 în H2SO4 (puteți găsi și alte formule oleum).
Un fapt uimitor! Oleumul este chimic mai activ decât acidul sulfuric concentrat, dar în ciuda acestui fapt, nu reacționează cu oțelul! Din acest motiv, este mai ușor de transportat decât acidul sulfuric în sine.Utilizarea „reginei acizilor” este cu adevărat mare și este dificil de spus despre toate modurile în care este utilizată în industrie. De asemenea, este utilizat ca emulgator în industria alimentară, pentru purificarea apei, în sinteza explozivilor și în multe alte scopuri.
Istoria apariției acidului sulfuric
Cine dintre noi nu a auzit niciodată de sulfatul de cupru? Deci, a fost studiat în antichitate și, în unele lucrări de la începutul noii ere, oamenii de știință au discutat despre originea vitriolului și despre proprietățile lor. Vitriolul a fost studiat de medicul grec Dioscoride, cercetătorul roman al naturii Pliniu cel Bătrân, iar în scrierile lor au scris despre experimentele efectuate. În scopuri medicale, diferite substanțe vitriol au fost utilizate de vindecătorul antic Ibn Sina. Cum s-a folosit vitriolul în metalurgie, se spunea în lucrările alchimiștilor din Grecia antică Zosima din Panopolis.
Prima metodă de producere a acidului sulfuric este procesul de încălzire a alumului de potasiu și există informații despre acest lucru în literatura alchimică din secolul al XIII-lea. La acea vreme, compoziția alumului și esența procesului nu erau cunoscute de alchimiști, dar deja în secolul al XV-lea, sinteza chimică a acidului sulfuric a început să fie tratată în mod intenționat. Procesul a fost după cum urmează: alchimiștii au tratat un amestec de sulf și sulf de antimoniu (III) Sb2S3 în timp ce se încălzeau cu acid azotic.
În epoca medievală în Europa, acidul sulfuric era numit „ulei de vitriol”, dar apoi numele s-a schimbat în acid vitriol.
În secolul al XVII-lea, Johann Glauber a obținut acid sulfuric ca urmare a arderii azotatului de potasiu și a sulfului nativ în prezența vaporilor de apă. Ca urmare a oxidării sulfului cu azotat, s-a obținut oxid de sulf, care a reacționat cu vapori de apă și, ca rezultat, s-a obținut un lichid de consistență uleioasă. Era ulei de vitriol și acest nume pentru acid sulfuric există și astăzi.
Farmacistul londonez Ward Joshua a folosit această reacție pentru producția industrială de acid sulfuric în anii treizeci ai secolului al XVIII-lea, dar în Evul Mediu consumul său era limitat la câteva zeci de kilograme. Domeniul de utilizare a fost restrâns: pentru experimentele alchimice, purificarea metalelor prețioase și în farmacie. Cantități mici de acid sulfuric concentrat au fost folosite la fabricarea chibriturilor speciale care conțin sare de dantelă.
În Rusia, abia în secolul al XVII-lea a apărut acidul vitriol.
În Birmingham, Anglia, John Roebuck în 1746 a adaptat metoda de mai sus pentru producerea acidului sulfuric și a început producția. Procedând astfel, a folosit camere mari cu plumb puternice, care erau mai ieftine decât recipientele din sticlă.
În industrie, această metodă și-a menținut poziția timp de aproape 200 de ani, iar în camere s-a obținut 65% acid sulfuric.
De-a lungul timpului, englezul Glover și chimistul francez Gay-Lussac au îmbunătățit procesul în sine, iar acidul sulfuric a fost obținut cu o concentrație de 78%. Dar pentru producerea, de exemplu, a coloranților, un astfel de acid nu a fost potrivit.
La începutul secolului al XIX-lea, au fost descoperite noi modalități de oxidare a dioxidului de sulf în anhidridă sulfurică.
Inițial, acest lucru a fost făcut folosind oxizi de azot, iar apoi platina a fost utilizată ca catalizator. Aceste două metode de oxidare a dioxidului de sulf au fost dezvoltate în continuare. Oxidarea dioxidului de sulf pe platină și pe alți catalizatori a ajuns să fie numită metoda de contact. Iar oxidarea acestui gaz cu oxizi de azot se numește metoda azotată pentru producerea acidului sulfuric.
Comerciantul britanic cu acid acetic Peregrine Phillips a brevetat doar un proces economic pentru producerea oxidului de sulf (VI) și a acidului sulfuric concentrat abia în 1831 și el este cel care este cunoscut lumii astăzi ca metodă de contact pentru producerea acestuia.
Producția de superfosfați a început în 1864.
În anii optzeci ai secolului al XIX-lea în Europa, producția de acid sulfuric a ajuns la 1 milion de tone. Principalii producători sunt Germania și Anglia, producând 72% din volumul total de acid sulfuric din lume.
Transportul acidului sulfuric
Transportul acidului sulfuric este o întreprindere laborioasă și responsabilă.
Acidul sulfuric aparține unei clase de substanțe chimice periculoase și, în contact cu pielea, provoacă arsuri severe. În plus, poate provoca otrăviri chimice la om. Dacă anumite reguli nu sunt respectate în timpul transportului, atunci acidul sulfuric, datorită explozivității sale, poate provoca multe daune atât oamenilor, cât și mediului.

Acidul sulfuric este clasificat ca periculos 8 și trebuie transportat de profesioniști special instruiți și instruiți. O condiție importantă pentru livrarea acidului sulfuric este respectarea Regulilor special dezvoltate pentru transportul mărfurilor periculoase.
Transportul rutier se efectuează în conformitate cu următoarele reguli:
- Pentru transport, containerele speciale sunt fabricate dintr-un aliaj special de oțel care nu reacționează cu acidul sulfuric sau cu titanul. Astfel de recipiente nu sunt oxidate. Acidul sulfuric periculos este transportat în rezervoare chimice speciale pentru acid sulfuric. Ele diferă prin design și în timpul transportului sunt selectate în funcție de tipul de acid sulfuric.
- La transportul acidului fumigant se folosesc rezervoare termice izoterme specializate, în care se menține regimul de temperatură necesar pentru a păstra proprietățile chimice ale acidului.
- Dacă se transportă acid obișnuit, atunci se selectează un rezervor de acid sulfuric.
- Transportul acidului sulfuric pe șosea, cum ar fi fumigant, anhidru, concentrat, pentru baterii, glover, se efectuează în containere speciale: rezervoare, butoaie, containere.
- Transportul mărfurilor periculoase poate fi efectuat numai de șoferii care au în mână un certificat ADR.
- Timpul de călătorie nu are restricții, deoarece în timpul transportului trebuie să respectați cu strictețe viteza permisă.
- În timpul transportului, este construit un traseu special, care ar trebui să ruleze, ocolind locurile aglomerate și facilitățile de producție.
- Transportul trebuie să aibă marcaje speciale și semne de pericol.
Proprietăți periculoase ale acidului sulfuric pentru oameni
Acidul sulfuric prezintă un pericol crescut pentru corpul uman. Efectul său toxic apare nu numai la contactul direct cu pielea, ci și la inhalarea vaporilor săi, când se eliberează dioxid de sulf. Expunerea periculoasă se extinde la:
- Sistemul respirator;
- Tegumentele pielii;
- Membrana mucoasă.
Arsenicul, care este adesea parte a acidului sulfuric, poate crește intoxicația corpului.
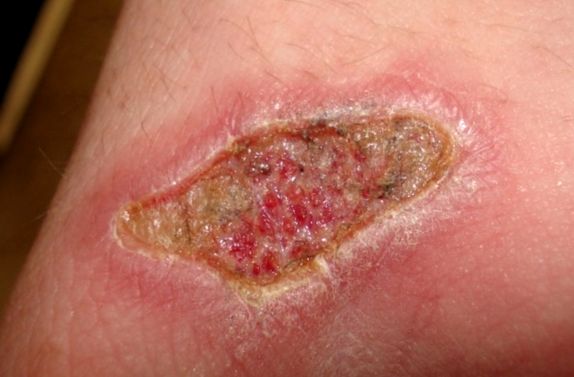
Important! După cum știți, arsurile severe apar atunci când acidul intră în contact cu pielea. Intoxicația cu vapori de acid sulfuric nu este mai puțin periculoasă. Doza sigură de acid sulfuric în aer este de numai 0,3 mg pe 1 metru pătrat.Dacă acidul sulfuric ajunge pe membranele mucoase sau pe piele, apare o arsură severă, care nu se vindecă bine. Dacă amploarea arsurii este impresionantă, victima dezvoltă o boală de arsură, care poate duce chiar la moarte dacă nu se acordă asistență medicală calificată în timp util.
Important! Pentru un adult, doza letală de acid sulfuric este de numai 0,18 cm3 pe 1 litru.Desigur, este problematic să „experimentăm” efectul toxic al acidului în viața de zi cu zi. Cel mai adesea, otrăvirea cu acid apare din neglijarea siguranței industriale atunci când se lucrează cu o soluție.
Intoxicația în masă cu vapori de acid sulfuric poate apărea din cauza defecțiunilor tehnice de producție sau a neglijenței și are loc o eliberare masivă în atmosferă. Pentru a preveni astfel de situații, funcționează servicii speciale, sarcina cărora este de a monitoriza funcționarea producției în cazul în care este utilizat acid periculos.
Ce simptome se observă la intoxicația cu acid sulfuric
Dacă acidul a fost ingerat:
- Durere în zona organelor digestive.
- Greață și vărsături.
- Tulburarea scaunului ca urmare a tulburărilor intestinale severe.
- Salivație grea.
- Datorită efectelor toxice asupra rinichilor, urina devine roșiatică.
- Umflarea laringelui și a gâtului. Există șuierătoare, răgușeală. Poate fi fatală prin sufocare.
- Pe gingii apar pete maronii.
- Pielea devine albastră.
Cu o arsură a pielii, pot exista toate complicațiile inerente unei boli de arsură.
În caz de otrăvire cu vapori, se observă următoarea imagine:
- Arsuri ale membranei mucoase a ochilor.
- Nasul sângerează.
- Arsuri ale membranelor mucoase ale căilor respiratorii. În acest caz, victima are un simptom dureros puternic.
- Edem laringian cu simptome sufocante (lipsa oxigenului, pielea devine albastră).
- Dacă otrăvirea este severă, atunci pot exista greață și vărsături.
Este important să știți! Intoxicația cu acid după ingestie este mult mai periculoasă decât intoxicația prin inhalarea vaporilor.
Primul ajutor și procedurile terapeutice pentru înfrângerea acidului sulfuric
Procedați după cum urmează pentru contactul cu acid sulfuric:
- Sunați mai întâi la o ambulanță. Dacă lichidul pătrunde în interior, spălați stomacul cu apă caldă. După aceea, cu înghițituri mici, va trebui să beți 100 de grame de floarea soarelui sau ulei de măsline. În plus, ar trebui să înghiți o bucată de gheață, să bei lapte sau magnezie arsă. Acest lucru trebuie făcut pentru a reduce concentrația de acid sulfuric și pentru a atenua starea umană.
- Dacă acidul pătrunde în ochi, trebuie să le clătiți cu apă curentă, apoi să picurați cu o soluție de dicaină și novocaină.
- Dacă acidul pătrunde pe piele, clătiți bine zona arsă sub apă curentă și aplicați un bandaj cu sifon. Este nevoie de aproximativ 10-15 minute pentru a clăti.
- În caz de otrăvire cu vapori, trebuie să ieșiți în aer proaspăt și, de asemenea, să clătiți membranele mucoase afectate cu apă cât mai mult posibil.
Într-un spital, tratamentul va depinde de zona arsurilor și de gradul de otrăvire. Anestezia se efectuează numai cu novocaină. Pentru a evita dezvoltarea infecției în zona infecției, pacientului i se alege un curs de antibioterapie.
Pentru sângerările gastrice, plasma este injectată sau sângele este transfuzat. Sursa sângerării poate fi eliminată prin intervenție chirurgicală.
Fapte interesante despre acidul sulfuric
- Acidul sulfuric în forma sa pură de 100% apare în mod natural. De exemplu, în Italia, Sicilia, în Marea Moartă, puteți vedea un fenomen unic - acidul sulfuric se scurge chiar de jos! Și ceea ce se întâmplă este acesta: pirita din scoarța terestră servește în acest caz ca materie primă pentru formarea sa. Acest loc este, de asemenea, numit Lacul Morții și chiar și insectele se tem să zboare spre el.!
- După erupții vulcanice mari, picături de acid sulfuric pot fi adesea găsite în atmosfera terestră și, în astfel de cazuri, „vinovatul” poate aduce consecințe negative asupra mediului și poate provoca schimbări climatice grave.
- Acidul sulfuric este un absorbant activ de apă, prin urmare este utilizat ca desicant de gaze. Pe vremuri, pentru ca ferestrele să nu se aburească în camere, acest acid era turnat în borcane și plasat între paharul de deschideri al ferestrelor.
- Acidul sulfuric este principala cauză a ploilor acide. Principala cauză a ploilor acide este poluarea aerului cu dioxid de sulf, care, atunci când este dizolvat în apă, formează acid sulfuric. La rândul său, dioxidul de sulf este eliberat atunci când combustibilii fosili sunt arși. În ploile acide studiate în ultimii ani, conținutul de acid azotic a crescut. Motivul pentru aceasta este reducerea emisiilor de dioxid de sulf. În ciuda acestui fapt, acidul sulfuric rămâne principala cauză a ploilor acide.
Experimente interesante cu acid sulfuric
Vă oferim o selecție video de experimente interesante cu acid sulfuric.
Luați în considerare reacția acidului sulfuric atunci când este turnat în zahăr. În primele secunde când acidul sulfuric intră în balon cu zahăr, amestecul se întunecă. După câteva secunde, substanța devine neagră. Urmează partea distractivă. Masa începe să crească rapid și să urce din balon. La ieșire, obținem o substanță mândră, similară cu cărbunele poros, care depășește volumul inițial de 3-4 ori.
Autorul videoclipului sugerează compararea reacției Coca-Cola cu acidul clorhidric și acidul sulfuric. Când se amestecă Coca-Cola cu acid clorhidric, nu se observă modificări vizuale, dar când se amestecă cu acid sulfuric, Coca-Cola începe să fiarbă.
O interacțiune interesantă poate fi observată atunci când acidul sulfuric intră pe hârtia igienică. Hârtia igienică este compusă din celuloză. Când acidul lovește, moleculele de celuloză sunt distruse instantaneu odată cu eliberarea de carbon liber. O carbonizare similară poate fi observată atunci când acidul ajunge pe lemn.
Am adăugat o bucată mică de potasiu în balon cu acid concentrat. În prima secundă, se eliberează fum, după care metalul se aprinde instantaneu, se aprinde și explodează, rupându-se în bucăți.
În experimentul următor, când acidul sulfuric lovește un meci, acesta se aprinde. În a doua parte a experimentului, este imersată o folie de aluminiu cu acetonă și un chibrit în interior. Folia este încălzită instantaneu cu eliberarea unei cantități uriașe de fum și dizolvarea completă a acestuia.
Un efect interesant se observă atunci când bicarbonatul de sodiu se adaugă la acidul sulfuric. Bicarbonatul de sodiu devine galben instantaneu. Reacția are loc cu o fierbere violentă și o creștere a volumului.
Vă sfătuim categoric să nu efectuați acasă toate experimentele de mai sus. Acidul sulfuric este o substanță foarte agresivă și toxică. Astfel de experimente trebuie efectuate în încăperi speciale dotate cu ventilație forțată. Gazele eliberate în reacțiile cu acidul sulfuric sunt foarte toxice și pot provoca leziuni ale tractului respirator și otrăvire. În plus, experimente similare sunt efectuate în echipamentul de protecție personală pentru piele și organele respiratorii. ai grijă de tine!